Перші ознаки апластичної анемії, клінічні рекомендації і причини виникнення
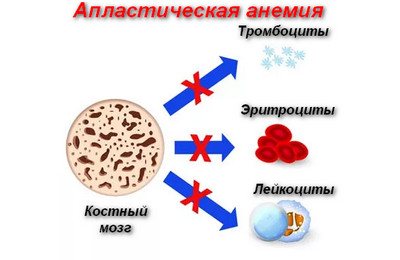
Перші ознаки апластичної анемії, клінічні рекомендації і причини виникнення Апластичну анемією називають хвороба, при якій порушується робота кровотворної системи. Можна навіть сказати, що це ціла група патологічних станів, які являють собою самостійну форму захворювання.
При цьому захворюванні кістковий мозок перестає виробляти клітини крові в необхідній кількості: лейкоцити, тромбоцити і еритроцити. Різні види хвороби протікають по-різному, деякі з них дають про себе знати відразу, а решта виявляються тільки через час.
Класифікація за МКБ
- D61.0 Конституціональна (включаючи спадкові форми).
- D61.1 Медикаментозна (окремий код присвоюється вражаючій ліків).
- D61.2 Викликана зовнішніми причинами, виключаючи медикаменти.
- D61.3 Ідіопатична, якщо причини невідомі.
- D61.8 Інші форми з уточненими факторами.
- D61.9 неуточнений форма.
Причини гіпопластична анемія
Причини можна розділити на три групи:
- Генетичні (пов’язані з генної передачею від одного з батьків, хромосомніаберації та ін.)
- Основні фактори пригнічення кісткового мозку (препарати хіміотерапії, радіаційний вплив, бензол (його похідні), миш’як)
- Рідкісні чинники, здатні в тій чи іншій мірі впливати на кістковий мозок – лікарські препарати (антибактеріальні засоби, протисудомні, транквілізатори, антитиреоїдні та інші), туберкульоз, вагітність.
Виділяють три групи головних причин розвитку гіпопластична анемія:
- Генетична. Спадковий фактор забезпечує передачу батьківських генів, що обумовлюють формування анемії, або деструктуризація хромосом, коли під впливом різних причин виникають хромосомні аберації, які проявляються подвоєнням, розривом, випаданням, перестановкою їх ланцюгів. Людина в нормі має 46 хромосом, при описаних порушеннях їх число може змінюватися (45, 47), що проявляється різними хромосомними захворюваннями та синдромами.
- Основна. До цієї групи відносять вплив радіаційного випромінювання, хіміотерапевтичних засобів, хімічних сполук на основі бензолу і миш’яку, аутоімунні захворювання.
- Рідкісна. До цієї категорії зараховуються лікарські препарати, побічна дія яких може проявлятися розвитком гіпопластична анемія. Це такі засоби, як протисудомні, сульфаніламідні, НПЗЗ (нестероїдні протизапальні), антибіотики, антитоксичні (при запальних процесах в щитовидній залозі), транквілізатори. Грибкові захворювання, туберкульоз, інфекції вірусної етіології, вагітність також можуть стати причиною недуги.
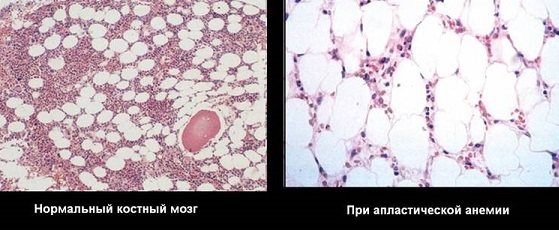
Механізм пошкодження кісткового мозку полягає в тому, що під дією перерахованих вище причин відбувається зміна хромосомного набору, що викликає порушений синтез ДНК. Освіта клітин крові гальмується і тканину червоного кісткового мозку заміщується жировою, яка не здатна виконувати продукує функцію. Загальний стан хворого погіршується, а картина крові представляється панцитопенией.
клінічна класифікація
Клінічна класифікація ділить всі види апластичної анемії на спадкові та набуті.
До спадкових відносять анемії з повною поразкою кровотворення, мають 2 підвиди:
- Фанконі – в поєднанні з вродженими вадами розвитку;
- Естра-Дамешека – без вад.
А також анемію з частковим або виборчим ураженням тільки еритроцитарного паростка (Даймонда-Блекфена).
Придбана апластична анемія (гіпопластична) включає випадки:
- гострого, підгострого і хронічного гноблення загального виробництва клітин крові;
- з ураженням тільки еритроцитів – парциальную, красноклеточная анемію.
Класифікація
Крім різних етіологічних варіантів апластичної анемії (лікарського, Постгепатитних, ідіопатичного), розрізняють гостру (до 1 міс. Течії), підгостру (від 1 до 6 міс.) І хронічну (більше 6 міс.) Форму захворювання. На підставі вираженості тромбоцитопенія і гранулоцитопении апластична анемія поділяється на 3 ступеня тяжкості:
- дуже важку (тромбоцитів менш 20,0х109 / л; гранулоцитів менше 0,2х109 / л)
- важку (тромбоцитів менш 20,0х109 / л; гранулоцитів менше 0,5х109 / л), за даними трепанобиопсии – низька клітинної кісткового мозку (менше 30% від норми)
- помірну (тромбоцитів більш 20,0х109 / л; гранулоцитів більше 0,5х109 / л)
Апластичну анемію, що протікає з виборчим пригніченням еритропоезу, називають парціальної красноклеточной аплазией.
причини
За різними статистичними даними, конкретні причини не вдається встановити в 49-78% випадків захворювання.
Найбільш вивченими виявилися вроджені форми: при анемії Фанконі зафіксовано чітку зв’язок зі змінами в парних хромосомах №1 і №7. У випадках анемії Даймонда-Блекфена виявлені мутації генів № 1, 16, 19 і 13. Можливими активаторами вважають вплив вільних радикалів-окислювачів.
Інші причини ділять на зовнішні і внутрішні.
Екзогенні (зовнішні) включають:
- Хімічні агенти – похідні бензолу, ртуті, нафтопродукти.
- Фізичний вплив проникаючої радіації.
- Лікарські препарати – протитуберкульозні засоби (Ізоніазид, ПАСК), Анальгін, цитостатики, сульфаніламіди, деякі антибіотики (Стрептоміцин, Тетрациклін, Левоміцетин).
- Інфекція – в ряді випадків доведено зв’язок з перенесеними інфекційними захворюваннями (грип, ангіну, мононуклеоз), переважною дією на клітини крові мають віруси гепатиту С, герпесу, Епштейна-Барра, цитомегаловірус.
До внутрішніх причин відносяться:
- ендокринні порушення – виявлений зв’язок зі зниженою функцією щитовидної залози, кістозними змінами яєчників у жінок;
- імунні зрушення – в зв’язку з втратою в літньому віці регулюючої ролі тимуса (вилочкової залози).
Більшість вчених дотримується думки, що у хворої людини, крім одного чи більше факторів, формується індивідуальна реакція на антигени.
Про роль ендокринних змін говорить досягнення тривалої ремісії у жінок з виявленою апластичну анемію під час вагітності, перериванням за медичними показаннями.
Причини і фактори ризику
Приблизно у половини пацієнтів встановити причину не вдається. У цьому випадку говорять про ідіопатичною (криптогенной) апластичної анемії. На даний момент відомі наступні фактори, що провокують розвиток захворювання:
- вплив іонізуючого випромінювання;
- імунні захворювання (симптомокомплекс «трансплантат проти господаря», еозинофільний фасциит, Тімом і карцинома тимуса);
- накопичення в тканинах солей важких металів (ртуті, срібла, міді, цинку, вісмуту, свинцю);
- тривалий виробничий контакт з ароматичними вуглеводнями (наприклад, бензолом), лакофарбовими складами, пестицидами, хлорорганічними сполуками;
- перенесені раніше інфекційно-запальні захворювання (грип, гепатит, цитомегаловірусна інфекція, СНІД, сепсис, туберкульоз, бруцельоз, лейшманіоз та ін.);
- терапія деякими лікарськими препаратами (пірамідон і похідними піразолонового ряду, Левоміцетином, сульфаніламідами, цитостатиками, імунодепресантами, препаратами золота, антитиреоїдними засобами, анальгін, індометацин, протисудомними препаратами).
На можливу наявність предрасполагающего генетичного дефекту, що приводить до розвитку апластичної анемії, вказує факт підвищеної зустрічальності у хворих антигену HLA-DR2, при цьому частота виявлення антигену DR у батьків хворих вище очікуваної. У дітей з важкою апластичну анемію виявлено досить істотне збільшення частоти антигену HLA-DPw3.
Під впливом перерахованих факторів в організмі запускається каскад патологічних реакцій:
- пригнічення імунітету;
- порушення метаболізму і запуск програмованої загибелі стовбурових клітин крові;
- ураження стовбурної гемопоетичної клітини, джерела освіти всіх видів клітин крові;
- ушкодження мікрооточення стовбурової гемопоетичної клітини, що приводить до збільшення порушення її функцій;
- вкорочення життя еритроцитів.
[Adsen]
патогенез захворювання
Апластична анемія викликана придушенням процесу виробництва кров’яних тілець в кістковому мозку. Можливий підвищений рівень руйнування і знищення клітин власними антигенами. Вивчається механізм апоптозу (самовільного нищівного процесу еритроцитів). Його прирівнюють до «запрограмованому суїциду». Встановлено підвищену активність ферментів деструктивної дії в крові, дефіцит нуклеїнових кислот.
Руйнування еритроцитів спостерігається усередині кісткового мозку на всіх рівнях дозрівання. Знижується тривалість життя червоних кров’яних клітин.
Оскільки утилізація заліза порушується, надлишки відкладаються в печінці і селезінці.
Утворюється підвищення рівня гормону еритропоетину, але кістковий мозок не реагує на його накази.
Зі зниженням гранулоцитів блокується їхня функція щодо участі в імунному захисті організму. Відповідне прояв зниженою згортання відбувається через тромбоцитопенічного синдрому.
Кількість лімфоцитів збільшено. Кістковий мозок стає «порожнім» (панміелофтіз).
Виражений недолік кисню в тканинах викликає дистрофічні зміни у внутрішніх органах. Особливо страждають ендокринні залози.
причини розвитку
Гіпопластична анемія може бути обумовлена негативною дією різних факторів, їх сукупність сприяє не тільки розвитку хвороби, а й призводить до збільшення перебігу патологічного процесу.
Дуже часто цей вид анемії виникає внаслідок токсичної дії деяких медикаментів, здатних спровокувати порушення в кістковому мозку з подальшою дисфункцією паростків кровотворення. Її формування не залежить від дозування медикаментів і від тривалості терапевтичного курсу.
До препаратів, здатним викликати порушення в системі кровотворення, відносять:
- сульфаніламіди,
- антибіотики,
- антигістамінні,
- тетрациклін.

Дуже часто недуга визначають у осіб, які тривалий час приймають Левоміцетин
Порушення гемопоезу спостерігається після курсу хіміотерапії, так як токсична дія препаратів руйнує не тільки патологічні утворення, а й здорові клітини і тканини.
Причинами розладу кровотворної функції також є аутоімунні хвороби, при яких імунний механізм спрямований на пригнічення не тільки патогенних мікроорганізмів, але і на власне пошкодження елементів кісткового мозку.
Таким чином, розрізняють три групи основних причин, що викликають порушення кровотворної функції кісткового мозку:
- Спадкова. Передача генетично модифікованих генів, що виявляється хромосомними аномаліями.
- Основна. Токсична дія хіміопрепаратів, радіаційне випромінювання, отруєння миш’яком і бензолом.
- Рідкісна. Формується на тлі прийому деяких медикаментів, при інфікуванні грибком.
Фактори, що провокують розвиток захворювання:
- гепатит вірусного походження;
- вірус герпесу;
- цитомегаловірусна інфекція;
- ВІЛ інфекція.
Іонізуюче випромінювання, що застосовується в ході рентгенологічного дослідження, грає важливу роль в механізмі формування анемії. Найчастіше дана патологія зустрічається у працівників рентгенологічних кабінетів, а також у пацієнтів, які пройшли курс радіохвильової терапії.
Клінічні прояви в дитячому віці
Симптоми апластичної анемії спадкового походження залежать від форми хвороби.
При анемії Фанконі у дитини виявляються вроджені дефекти в кістковій системі (немає першого пальця на кисті руки, викривлені або відсутні променеві кістки). До пороків додаються аномалії серця і нирок, маленькі очні яблука.
Рекомендуємо почитати: Ознаки залізодефіцитної анемії
Апластична анемія у дітей починає проявлятися з чотирьох років, рідше в ранньому віці. Дитина скаржиться на головні болі, втому. Схильний до частих простудних інфекцій, носових кровотеч. При обстеженні виявляють характерну картину крові. Хвороба набуває хронічного перебігу з періодами загострень.
Летальний результат можливий від приєднання інфекції або гострої кровотечі.
При анемії Естра-Дамешека спостерігається тільки патологія крові. Випадки дуже рідкісні.
Анемія Даймонда-Блекфена вражає виключно еритроцитарний паросток крові. Рідше спостерігалися зміни кісток скелета і очей. Кровоточивість відсутня. Шкірні покриви бліді з сіруватим відтінком. Рано збільшується селезінка та печінка. В аналізі крові рівень тромбоцитів і лейкоцитів знижується тільки при значному ураженні селезінки. Звичайне співвідношення лейкоцитів і еритроцитів у хворого 100: 1 при нормі до 4: 1. Хронічне важкий перебіг хвороби не дозволяє дожити до 20-ти років.
Загальні поняття про гіпопластична анемія
Гипопластической анемією є патологічна зміна картини крові внаслідок придушення роботи червоного кісткового мозку. Проявляється це зниженням вироблення всіх паростків крові (еритроцитарного, лейкоцитарного, тромбоцитарного) або лише червоного (зменшення еритроцитів). Історія першого опису і появи даного захворювання починається з 1888 року.
В цей час П. Ерліх виявив у дівчини хвороба, яка виявляється гострим розвитком кровоточивості, лихоманки, глибокої анемії і лейкопенії. За результатами розтину і дослідження кісткового мозку, ознак порушення кровотворення виявлено не було. Анапластична анемія як самостійне захворювання виділено Шоффаром в 1904 р Пізніше з’явилася апластична анемія за типом Ерліха з симптомами сепсису, некрозу, геморагії і аплазії (відсутність всіх паростків кровотворення в кістковому мозку), що виявляється у молодих людей (18-20 років).
Основним контингентом, що страждають від цього захворювання, є юні дівчата і діти. У патогенезі розвитку виділяють кілька етапів. Спочатку тканини, внаслідок нестачі кисню і поживних речовин, атрофуються і втрачають свої функції. Далі жирова і сполучна тканини заміщають загиблі клітини, що призводить до поширення патологічного процесу. Прогресування захворювання відбувається дуже швидко і в разі відсутності терапії може призвести до смерті.
Прояви придбаної анемії
Симптоми апластичної анемії проявляються в періоди загострення, а хвороба набуває прогресуюче повільний плин. Всі ознаки можна поділити на основні синдроми, в залежності від гноблення конкретного паростка клітин крові.
- Анемія – характеризується вираженою слабкістю, скаргами на запаморочення, шумом у вухах, нападами серцебиття, задишкою.
- Геморагічні прояви – на шкірі видно синці, не пов’язані з травмуванням, ясна пухкі і кровоточать. Пацієнтів турбують часті носові кровотечі. У важких випадках можливе крововилив в мозок.
- Знижений рівень гранулоцитів викликає падіння захисних імунних механізмів. Пацієнти часто заражаються інфекційними хворобами. Будь-які поранення у них ускладнюються приєднанням нагноєння навколишніх тканин. Ангіна протікає в виразково-некротичної формі. Після ін’єкцій утворюються абсцеси. Стоматит призводить до виразок в порожнині рота. Важким ускладненням є загальний сепсис.
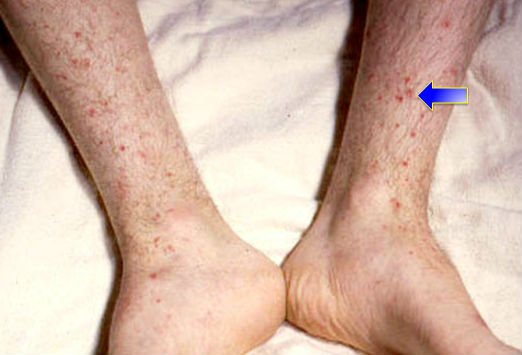
геморагічні висипання
При огляді лікар звертає увагу на блідість шкіри, синюшність губ, синці на тілі, іноді мелкоточечную висип.
Артеріальний тиск знижений. Прослуховується характерний шум в серці, частота скорочень вище норми.
Збільшення печінки відбувається у важкій стадії, залежить від вираженості серцевої недостатності.
симптоми
Залежно від того, наскільки виражені порушення процесів кровотворення, клінічні прояви і симптоми апластичної анемії дуже різноманітні: розрізняють перехідні форми апластичної анемії від часткового пригнічення процесів утворення клітин крові до вираженого недорозвинення кісткового мозку.
У перебігу захворювання виділяють 3 основних синдрому апластичні анемій:
- цітопеніческім;
- септик – некротичний;
- геморагічний.
Ці синдроми анемії можуть по-різному проявлятися в організмі людини в залежності від ступеня розвитку захворювання. Розрізняють 3 етапи розвитку хвороби, при цьому симптоми апластичної анемії на кожному з них різняться.
I етап характеризується проявом неспецифічних симптомів, які можуть бути при будь-якому іншому патологічному процесі, – хронічна втома і загальна слабкість. Дуже часто хворі пристосовуються до існуючої у них анемії і звертаються до фахівця тільки тоді, коли захворювання почне прогресувати. Також цей етап характеризується такими проявами геморагічного синдрому, як маточне, носова кровотеча і підвищена схильність до утворення синців (синці на тілі без причини).
На II етапі у хворих хворіють на апластичну анемію відзначається блідість шкіри і видимих слизових оболонок, також іноді можуть виникати синці. Якщо захворювання переходить в гостру форму, крім блідості шкірних покривів також спостерігають геморагічний шок, некроз слизових оболонок і високу температуру. В організмі активізуються різні запальні процеси (зокрема, пневмонія).
Зазвичай печінка і селезінка не збільшуються, але якщо діагностують аутоімунних форму апластичної анемії, при яких в організмі хворого виробляються антитіла до еритроцитом, може розвинутися помірна спленомегалія (збільшення селезінки) і легка жовтушність шкіри та склер, викликаних наявністю в крові гемолитических компонентів.
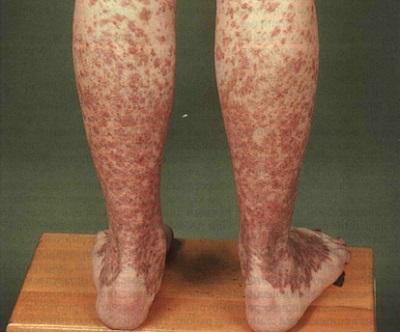
геморагічні висипання
Показники в аналізі крові
Найбільш яскраво вираженим є III етап анемії, який характеризується бурхливим картиною клінічних проявів. На цій стадії розвитку апластичної анемії аналіз крові показує:
- в клінічному аналізі крові визначається яскраво виражена анемія (як правило, нормохромна) – рівень гемоглобіну зменшується до 20 – 30 г / л, концентрація ретикулоцитів знижується (говорить про зниження функціональності кісткового мозку);
- виникає лейкопенія, гранулоцитопенія, тобто різко знижується рівень вмісту в крові гранулярних лейкоцитів. При цьому кількість лімфоцитів не змінюється;
- зниження тромбоцитів, аж до нуля;
- при гістологічному дослідженні тканини кісткового мозку відзначається катастрофічне зникнення його клітин, які заміщуються жировою тканиною;
- різко підвищується ШОЕ – до 30 – 50 мм / год;
- в сироватці крові концентрація заліза збільшується.
Перебіг хвороби
Клінічний перебіг апластичної анемії відрізняється за формою хвороби.
гостра анемія
Гостра форма захворювання протікає бурхливо, починається різко з вираженого геморагічного синдрому (кровотечі різних видів). Приєднується інфекція з високою температурою (ангіна, запалення легенів). Через кілька днів настає крайня ступінь спустошення кісткового мозку, пригнічення еритроцитарного паростка. У крові виявляється відносний лімфоцитоз, значне прискорення ШОЕ. Летальний результат наступає через 1-1,5 місяці.
подострая форма
Протікає менш швидко. Чи не занадто виражені геморагії. Критичні зміни крові настають через 3 місяці або рік.
хронічна форма
Хвороба починається поступово і повільно прогресує. У людини з’являється запаморочення, блідість, непостійні синці. При огляді не визначається збільшення селезінки. Можлива пальпація хворобливих лімфовузлів. При правильному лікуванні вдається призупинити процес загибелі кісткового мозку. Ремісії тривають до декількох років. Загострення провокується будь-якою інфекцією, стресами.
Симптоми гіпопластична анемія
Симптоми найчастіше наростають поступово. Бурхливий гострий перебіг з яскравою симптоматикою виникає вкрай рідко.
Ранніми симптомами є:
- слабкість
- адинамія
- запаморочення
- Задишка при фізичному навантаженні
- Головний біль, рідше м’язова, в кістках і в області серця.
Далі з’являються видимі ознаки:
- Блідість шкірних покривів і видимих слизових (воскоподібний відтінок)
- Крововиливи в шкіру, слизові оболонки
- Кровотечі (зовнішні і внутрішні)
При більш пізніх стадіях розвиваються неврологічні відхилення (ослаблення рефлексів і ін.), Пов’язані з крововиливом в головний мозок.
![]()
Патогенез проявів даної хвороби пояснюється нездатністю клітин крові (через низький їх змісту) виконувати свої функції. Таким чином, поява геморагічного синдрому обумовлено тромбоцитопенией і пошкодженням судинної стінки (недолік серотоніну і гіпоксія призводить до підвищення її проникності).
До основних проявів геморагічного синдрому відносять:
- часті безпричинні носові кровотечі;
- поява синців і синців на шкірі при натисканні (пальцевая і манжеточной проба);
- кровотеча з ясен;
- жінки часто скаржаться на щедрість і подовження менструацій.
У разі тривалого патологічного процесу або при масивному пошкодженні тромбоцитів можуть розвиватися такі ускладнення, як профузне внутрішня кровотеча або інфаркт головного мозку з крововиливом. У підсумку це може призвести до смерті хворого.
Зниження імунітету і опірності до інфекційних агентів пов’язано з пригніченням лейкоцитарного паростка. Гіпопластична анемія з імунодефіцитом представлена наступними симптомами:
- Костномозговой аплазией.
- Ниркової гіпоплазією.
- Мікроцефалією.
- Скелетними деформаціями.
Дитина більш схильний до таких змін, оскільки його організм перебуває на стадії активного зростання і розвитку всіх систем. Захворювання схильне до хронізації процесу з періодичними загостреннями.
Зменшене утворення еритроцитів призводить до розвитку анемічного симптомокомплексу:
- Втома, зниження працездатності.
- Синкопальні стани (проявляються непритомністю), миготіння мушок перед очима, запаморочення.
- Скарги на задишку в спокої і при низькій фізичному навантаженні.
- Головний біль.
- Порушений сон.
- Дискомфорт за грудиною (біль, відчуття тиску, поколювання).
- Прискорене серцебиття (понад 90 ударів в хвилину).
- Знижений апетит.
- Втрата у вазі.
- Сухість, блідість, мармуровість шкіри.
У разі виявлення гостро протікає важкої форми захворювання прогноз у такого пацієнта несприятливий: смерть настає протягом 3 місяців. Частою причиною летальності є внутрішні кровотечі або персистуючі інфекції, що призводять до сепсису.
Вітамін А (ретинол, антіксерофтальміческій фактор) міститься тільки в продуктах тваринного походження. Особливо багато його в нирках і печінці тріскових риб, китів, тюленів, дельфінів. У продуктах рослинного походження вітамін А знаходиться в вигляді провітаміну – каротину.
Джерел вітаміну є продукти тваринного походження – яєчний жовток, молоко, масло, сир, тріска, палтус, печінку ссавців (містять ретинолу пальмітат) і рослинного походження – морква, шпинат, цибуля, чорна смородина, абрикоси, чорниця (вітамін А представлений каротиноїдами).
Вітамін А стійкий при звичайному варінні, але руйнується при високій температурі, сушці і під впливом окислювачів.

Каротин стає біологічно активним лише після перетворення на вітамін А в стінці кишечника і печінки. Кожна молекула каротину є джерелом двох молекул вітаміну А.
Органом, що містить основні запаси вітаміну А, є печінка. Мобілізація вітаміну А з депо і транспорт його до органів-мішеней здійснюється ретінолсвязивающего білком, який виробляється в печінці.
Фізіологічні функції: світлова адаптація, цитопротекції і диференціація епітеліальних клітин, синтез глюкокортикоїдів, синтез холестеролу, зростання організму.
Майже весь вітамін А, що надходить з їжею, без змін проходить через шлунок і надходить в тонкий кишечник, де більша його частина піддається всмоктуванню і в складі хіломікронів по лімфатичних шляхах надходить в печінку. У печінки хиломікрони, що містять ефіри вітаміну А, піддаються розщепленню з утворенням вільного ретинолу.
Розрізняють специфічну і загальне системне дію вітаміну А. Перше проявляється в участі спиртової та альдегідної форм вітаміну в біологічних функціях зору і розмноження. В акті зору вітамін А бере участь завдяки освіті з білками-опсин в умовах темряви пурпур-родопсина. На світлі відбувається процес розкладання зорового пурпура та частина ретинолу при цьому втрачається. Для нормальної зорової функції необхідний постійний приплив ретинолу.
Картина крові і ступеня тяжкості
У периферичної крові, взятої з пальця, виявляють:
- зниження еритроцитів, зміна їх форми і розмірів;
- низький рівень гемоглобіну;
- зниження відносного і абсолютного кількості тромбоцитів і гранулоцитів;
- прискорену ШОЕ;
- відносний лімфоцитоз;
- зростання числа ретикулоцитів.
Помірно важкою формою анемії вважається хвороба з вмістом нейтрофілів від 0,2 до 0,5 х 109 в літрі крові.
До важких випадків відносять випадки при кількості гранулоцитів мене 0,5 х 109, тромбоцитів – менше 10 х 109, ретикулоцитів – до 1%; при цьому в костномозговом пунктате має бути клітин, що не утворюють кров’яні елементи, більше 65%, а попередників еритроцитарного паростка – одиниці.
Вкрай важкою називають стадію хвороби, якщо нейтрофілів менше 0,2 х 109.
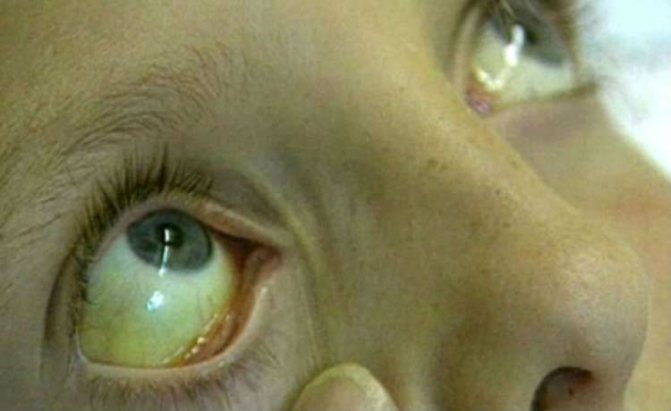
Желтушность склер при збільшеною печінки
Від яких хвороб слід відрізняти апластичну анемію
Пригнічення кісткового мозку виявляється не тільки при апластичної анемії, але і при інших захворюваннях. Правильно визначити діагноз допомагає зіставлення симптомів і результатів обстеження.
- Лейкози – частіше виявляється збільшення селезінки, в кістковому мозку багато бластних клітин попередників лейкоцитів.
- Агранулоцитози – не викликають анемію і зниження тромбоцитів.
- Хвороби зі збільшенням печінки і селезінки – гепатити, цироз, тромбофлебіт селезінкової вени – виявляється жовтушність шкіри та склер, порушення печінкових проб.
- Рідкісне захворювання, пароксизмальна нічна гемоглобінурія (ПНГ) виникає у віці від 30 до 35 років. Викликана відсутністю певних видів білків. Клітини, в яких при проведенні іммунотіпірованія не знаходять цих структур, називають ПНГ клонами. Клінічно хвороба проявляється внутрішньосудинним гемолізом з кров’ю в сечі, зниженням гемоглобіну, підвищенням білірубіну, недостатністю клітин кісткового мозку. У 40% хворих спостерігається тромбоз великих вен і артерій. Це і є причиною смерті.
можливі ускладнення
При апластичної анемії можливі такі наслідки:
- різні кровотечі – геморагічні ускладнення. Найнебезпечніше ускладнення – геморагічний інсульт (певну ділянку головного мозку просочується кров’ю, в результаті чого гине);
- анемічних кома – відсутність реакції на те, що відбувається через втрату свідомості, що виникає в результаті надходження недостатньої кількості кисню до головного мозку, що викликано значним зниженням кількості еритроцитів;
- при наявності хронічних захворювань погіршується стан внутрішніх органів.
- ускладнення інфекційного характеру – розвиток захворювань, які викликані різними мікроорганізмами (бактерії, гриби, віруси);
Якщо при даному захворюванні не проводиться лікування, в 90% випадків пацієнт помирає протягом року.
Яке обстеження проводять для діагностики
У схему обстеження необхідно включити проведення наступних досліджень:
- загальний аналіз крові з підрахунком ретикулоцитів, тромбоцитів, визначенням гематокриту;
- група крові та резус-фактор пацієнта для підготовки до переливання крові;
- дослідження пунктату з кісткового мозку, а при підозрі на вроджені форми – кісток черепа;
- імунологічні аналізи на антитіла до клітин крові, визначення кількості імуноглобулінів, проведення реакції бласттрансформації лімфоцитів;
- біохімічні тести: білірубін і його форми; загальний білок з протеінограмма; «Печінкові проби» АЛТ, ACT; вміст сироваткового заліза;
- проведення рентгенографічного дослідження кісток черепа, грудної клітки, кистей рук;
- УЗД органів черевної порожнини дозволить визначити розміри печінки і селезінки.
Аналізами крові контролюють ефект від ліків
При підозрі на вроджене захворювання потрібно обстеження близьких родичів.
При наявності інфекційних прояви потрібна консультація стоматолога, отоларинголога, хірурга.
діагностика
Обстеження являє досить серйозні труднощі, оскільки надійних критеріїв поки немає, також лікарі обмежені у виборі методик. Завдання лягає на плечі гематолога.
Серед можливих заходів:
- Усне опитування хворого. Потрібно встановити всі присутні скарги, щоб скласти повну клінічну картину. Це важливо, оскільки дозволяє висунути гіпотези щодо стану людини.
- Збір анамнезу. Перенесені раніше хвороби, момент розвитку, почала симптоматичних проявів, шкідливі звички, спосіб життя, особливо важливо встановити сімейну історію хвороб.
- Загальний аналіз крові. Лабораторне дослідження використовується для оцінки концентрації формених клітин (еритроцитів), рівня гемоглобіну, інших показників. Досить інформативна методика незважаючи на простоту.
- Обов’язково проводиться дослідження біохімічне. Оцінці підлягають печінкові проби, рівні специфічних речовин: білірубіну, лужної фосфатази.
- Доброю методикою ранньої діагностики і верифікації діагнозу виступає пункція кісткового мозку для забору матеріалу (біопсія). Використовується найчастіше як крайній захід. З огляду на інвазивності (травматичності) застосовується не завжди.
- Можливе призначення консультації генетика. За свідченнями.
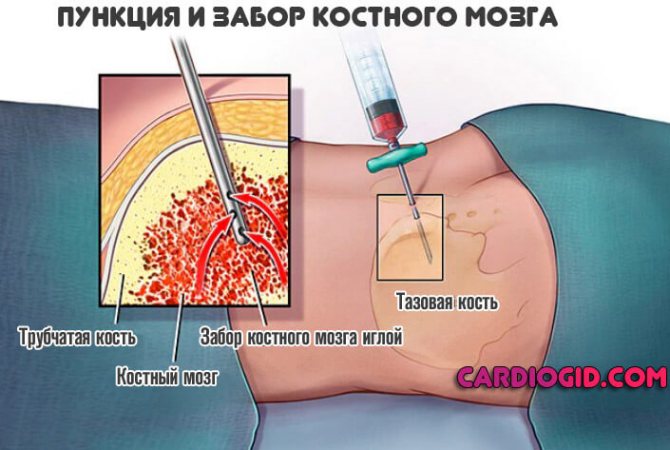
Діагностика вимагає терпіння, хоча час на повне обстеження є не завжди. У міру подальшого або повторного курсу можливий перегляд спочатку встановленого захворювання.
лікування
Лікування апластичної анемії, незважаючи на здаються однаковими симптоми, лікарі призначають в залежності від передбачуваного головного чинника в етіології хвороби.
Вперше виявлені випадки обов’язково лікуються в гематологічному відділенні стаціонарно. Тільки спеціалізована терапія дозволяє підібрати потрібну дозування і оптимальний препарат.
Основні методики:
- переливання донорської крові або окремих елементів з замісної метою;
- пересадка кісткового мозку;
- ліки, що активізують кровотворення.
Для переливання використовують цільну кров, еритроцитарної і тромбоцитарної масу, гранулоцити. Їх готують на «Станції переливання» з крові донорів. Метод вважається тимчасовим, оскільки просто заповнює відсутню кількість власних кров’яних клітин, але не діє на кістковий мозок. Якщо доведено аутоімунний механізм патології, його застосовувати не можна. Організм виробляє антитіла на чужорідні клітини.
Часті переливання призводять до накопичення заліза і його відкладенню у внутрішніх органах, порушуючи їх роботу. Це змушує додавати препарати, що сприяє виведенню заліза з крові.
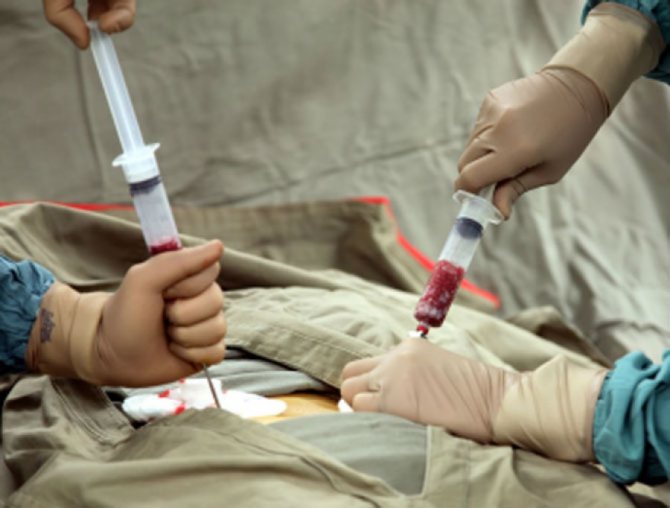
Забір кісткового мозку для трансплантації проводиться в умовах операційної проколами стегнової кістки, шприцами відсмоктується до 2л маси
Трансплантація кісткового мозку є найрезультативнішим способом лікування. Перед процедурою припиняють переливання крові, щоб знизити можливість відторгнення. Донором може стати родич з одногруппной кров’ю і індивідуальної сумісністю. Метод більш показаний в молодому віці пацієнта.
Перед пересадкою проводиться променева і хіміотерапія. Необхідно придушити можливий імунну відповідь на відторгнення стовбурових клітин донора. Метод проводиться тільки в спеціалізованих відділеннях, є дорогим.
Як імунодепресантів використовують: Циклоспорин, антімоноцітарний і антилімфоцитарну глобуліни. Комплексним препаратом цієї групи є Атгам (містить необхідні антіглобуліни). Він показаний у випадках неможливості пересадки кісткового мозку. Для попередження анафілактичних реакцій застосовують кортикостероїди.
Стимуляцію кровотворення в кістковому мозку здійснюють застосуванням таких препаратів, як Філграстим, Лейкомакс. Вони активізують вироблення гранулоцитів, тому показані тільки при лейкопенії. Курс лікування – два тижні.
Доведено здатність чоловічих статевих гормонів (андрогенів) стимулювати всі паростки крові. Для лікування чоловіків застосовуються тривалі курси Тестостерона пропионата, Сустанона.
Видалення селезінки дає ефект у 85% хворих. Метод заснований на механізмі припинення вироблення антитіл на власні клітини. Можна проводити всім пацієнтам, які не мають інфекційних ускладнень.

Ліки вводять переважно в ін’єкціях
Якщо у хворого є кровоточивість, вводяться кровоспинні засоби: Дицинон, Амінокапронова кислота.
Виведення заліза з організму домагаються за допомогою Десфералу.
Від лікування апластичної анемії народними засобами слід відмовитися. Ця патологія вимагає дуже вдумливого і точного обліку лікарських препаратів. А як можна прорахувати корисні складові в рослинах? Є згадки про стимулюючу дію часнику, лугового конюшини, редьки, моркви і буряка. Але воно настільки мало, що застосування тільки викликає необгрунтовані надії у пацієнтів і родичів.
Апластична анемія – механізм розвитку
В даний час існує три теорії, що пояснюють механізм розвитку апластичної анемії. Кожна з них отримала підтвердження в ході досліджень.
Увага. У деяких випадках жодна з існуючих теорій не може пояснити виникнення захворювання. При такому варіанті використовують назву «ідіопатична апластична анемія».
Тому офіційно теорії прийняті, але вивчення механізмів виникнення апластичної анемії триває.
Теорії патогенезу (виникнення) апластичної анемії:
- аутоімунна;
- стромальна;
- передчасний апоптоз.
аутоіммунна теорія
Довідково. У аутоімунної теорії за основу береться розвиток імунної відповіді до клітин кісткового мозку.
Виникла вона в результаті дослідження матеріалу биоптата кісткового мозку після розвитку апластичної анемії.
У великій кількості випадків вчені побачили присутність клітинного імунітету (моноцити, Т-кілери), а також факторів запалення – фактор некрозу пухлин, інтенферон альфа і гамма.
Після більш детального вивчення стало зрозуміло, що скупчуються вони через генної мутації. В результаті порушення роботи гена PIG-A виникає дефіцит спеціального глікопротеїну, який необхідний для того, щоб знижувати активність системи комплементу, що входить до складу імунної системи.
В результаті цієї поломки захист власних клітин кісткового мозку слабшає, вони починають сприйматися, як чужорідні і розвивається аутоімунна реакція. Залежно від кількості пошкоджених клітин ступінь вираженості симптомів різниться.
Важливо. Чим більше залучено тканини, тим агресивніша анемія спостерігається у пацієнта.
стромальна теорія

Нормальне функціонування механізму кровотворення багато в чому залежить від строми, тобто спеціального соединительнотканного підстави, в якому знаходяться клітини кісткового мозку.
Строма відповідає за вироблення спеціальних речовин (інтерлейкіни і фактори стовбурових клітин), які необхідні для направлення недиференційованих молодих клітин шляхом утворення еритроцитів, тромбоцитів або лейкоцитів.
Стимулюється ця вироблення еритропоетином.
У разі порушення виділення факторів росту на рівні строми виникають низькодиференційовані клітини, які не можуть виконувати свої функції. Вони не досягають диференціювання, достатньою для визначення в крові при аналізі.
Довідково. Підтверджується дана теорія при біопсії кісткового мозку – визначаються попередники клітин у великій кількості. А також визначається підвищений рівень еритропоетину в крові. Такі зміни характерні не більше ніж для 20% випадків.
Теорія передчасного апоптозу
Терміном апоптоз в медицині позначають природний процес загибелі клітини, коли вона в повному обсязі виконала свою функцію. Відбувається це у всіх тканинах організму. Після певного часу клітини піддаються мутації, починають сприйматися організмом, як старі, і видаляються.
У нормі процес являє собою захисний механізм, який сприяє оновленню тканин. Мутував клітини можуть переродитися в пухлинний процес, і функція апоптозу – не допустити цього. Однак, якщо цей процес починає відбуватися завчасно, можливо надмірне видалення клітин тканини. При недостатньому синтезі нових клітин цей процес призводить до порушення функції.
Довідково. Причиною занадто раннього видалення здорових і молодих клітин є мутація гена, що відповідає за вироблення протеїну Р-450.
Вивчення механізмів розвитку апластичної анемії досі є зоною наукових інтересів дослідників усього світу. Однак це може внести вклад в лікування захворювання в майбутньому, але ніяк не позначається на сучасних пацієнтах.
Справа в тому, що на сьогоднішній момент найефективнішим методом лікування апластичної анемії залишається пересадка кісткового мозку. Для уповільнення процесу використовують стероїдні гормони.
Увага. Жоден з методів лікування не враховує патогенез процесу.
прогноз
На сьогоднішній день так і не знайдено універсальний засіб лікування, тому прогноз для життя пацієнта залишається несприятливим. Найбільш висока смертність в групі хворих з важкою формою хвороби. Відновити кровотворення не вдається, а хворі гинуть від загального сепсису.
При менш тяжкому перебігу і хорошої реакції на пересадку стовбурових клітин і імунодепресанти позитивні результати отримують від половини до 90% випадків.
Без трансплантації кісткового мозку та застосуванні тільки імуноглобулінів і циклоспорину ремісія настає у 60% пацієнтів.
методи лікування
Лікування апластичної анемії – складний і комплексний процес, що вимагає активної участі лікаря і пацієнта. Для медикаментозної терапії можуть застосовуватися такі групи ліків:
- Антибіотики (Амікацин, Цефтриаксон, Тобраміцин). Призначаються при приєднанні бактеріальної інфекції.
- Цитостатики (імуран, Метотрексат, Циклофосфан). Призначають для лікування придбаних форм апластичної анемії.
- Імунодепресанти (Метилпреднізолон, Дексаметазон). Зменшують реакцію імунітету, дозволяючи кістковому мозку виробляти кров’яні клітини.
- Стимулятори кровотворення (Нейпоген, Лейкін). Підсилюють вироблення кров’яних клітин кістковим мозком.
Єдиним радикальним способом, що дозволяє взяти під контроль апластичну анемію і отримати позитивний результат, є трансплантація кісткового мозку. Така методика найбільш ефективна в молодому віці, але є одна складність – матеріал для пересадки повинен бути сумісний або частково сумісний з антигенними складом кісткового мозку хворого. В цьому випадку краще всього підходить найближчий родич пацієнта.
Перед пересадкою застосовують хіміотерапію, спрямовану на пригнічення захисних властивостей організму пацієнта. Подібний захід пов’язана з необхідністю запобігти відторгненню пересаджених клітин.
Для лікування патології, що супроводжується низьким значенням еритроцитів або тромбоцитів, можна застосовувати переливання крові. Методика не дозволяє позбавити від апластичної анемії, але захворювання буде взято під контроль фахівців, що позитивно позначиться на самопочутті хворого.
Про те, як проводиться переливання крові дітям, написано тут:
Галерея лікарських засобів
Цефтриаксон використовується для усунення інфекції імуран – препарат з групи цитостатиків Метотрексат може застосовуватися для лікування апластичної анемії завдяки своїм властивостям Філграстим допомагає кістковому мозку виробляти кров’яні клітини Метилпреднізолон зменшує реакцію імунної системи

